Proseguiamo, con questo articolo, la striscia informativa (Faq) che ha l’obiettivo di trasmettere, nella maniera più semplice possibile e usufruendo della bibliografia che la Scienza e il Diritto mettono a disposizione, risposte alle domande più frequenti a seguito della pandemia da Coronavirus. Curano questa rubrica, la dott.ssa Fernanda Annesi (Biologa CNR), l’avv. Erminia Acri e il dott. Giorgio Marchese (Medico Psicoterapeuta )
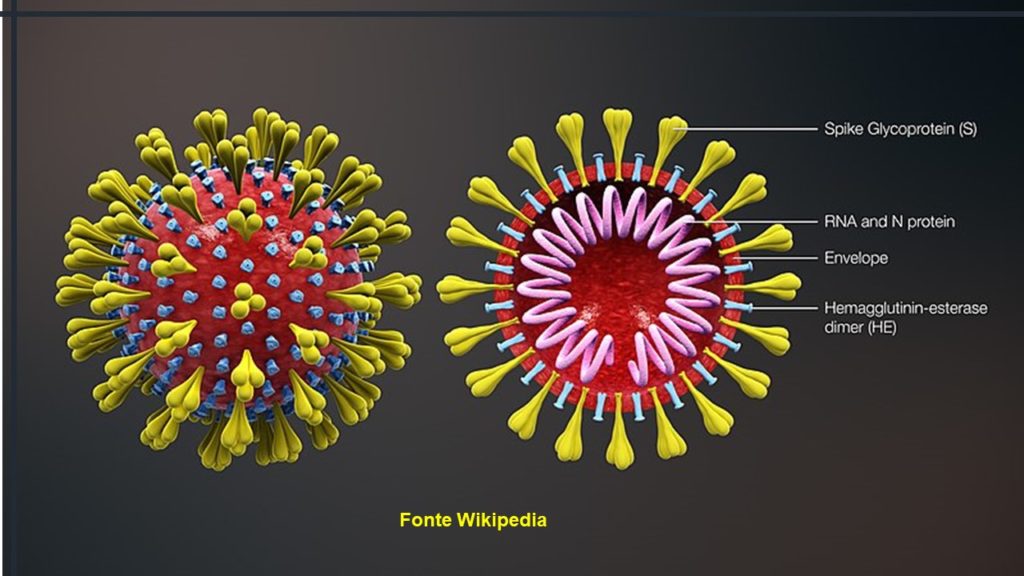
Come abbiamo visto nel precedente articolo, (tutti) i coronavirus hanno il genoma (cioè il materiale genetico con cui riescono a duplicarsi) costituto da RNA protetto da un struttura proteica chiamata nucleocapside, a sua volta ricoperto da un pericapside o mantello lipidico a cui sono associate altre proteine .
Tra queste, le proteine “spike” (chiamate anche “proteina S”) che hanno la capacità di fusione con la membrana cellulare e di creare una risposta anticorpale che provoca una reazione negativa sui globuli rossi chiamata agglutinazione (letteralmente “precipitato”) e che, quindi, sono responsabili dell’ingresso del virus nella cellula ospite, quindi essenziali nella fase iniziale dell’infezione e, anche di reazioni avverse nel sangue dell’ospite.

(Tutti) I coronavirus si attaccano alla membrana cellulare delle cellule bersaglio grazie, come abbiamo visto sopra, alle loro proteine S. Non è ancora chiaro se la penetrazione della cellula sia effettuata mediante fusione del pericapside (la parte del mantello che comprende le proteine “S”) con la membrana della cellula o per endocitosi (che sarebbe una specie di assorbimento attraverso la formazione di capsule).
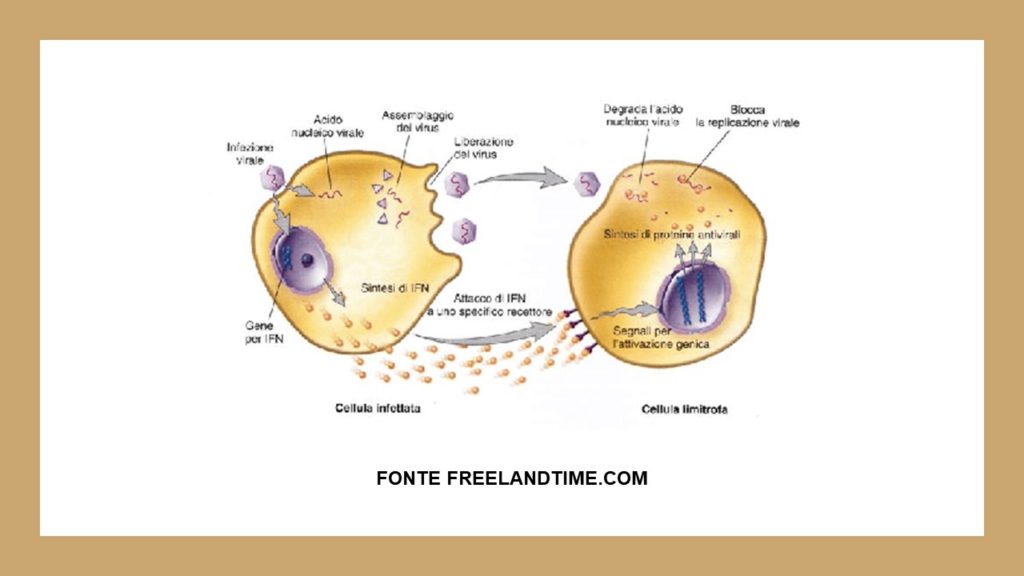
Come possiamo vedere nell’immagine sotto riportata, all’interno del citoplasma della cellula (tutta la porzione “fluida” della cellula contenuta all’interno della membrana) il coronavirus rilascia il suo RNA a singolo filamento positivo che si attacca ai ribosomi (i quali, prendendo spunto dal precedente articolo, sono paragonabili al cuoco che prepara la pietanza partendo dalla “comanda” del cameriere) dove questo RNA viene trasformato in messaggio adeguato a produrre proteine: quelle necessarie ad assemblare nuovi virus che, attraverso un condotto, chiamato “reticolo endoplasmatico” vengono rilasciati, all’esterno della cellula, con un meccanismo opposto a quello con cui vi sono entrati e che si chiama “esocitosi”.
Attualmente, a causa della complessità del materiale genetico di questo coronavirus e del ciclo di replicazione, la conoscenza scientifica dei fattori dell’ospite coinvolti è ancora in una fase iniziale rispetto a ciò che è noto per altri RNA virus, per cui alcuni passaggi spiegati prima (validi per altri RNA Virus) potrebbero risultare con qualche variante, alla luce di nuovi studi.(Fonte PubMed)
Come si nota, sempre dall’immagine riportata sotto, il meccanismo di produzione dei virus, fa rilasciare molto interferone.
Con questo nome generico si indica un gruppo di proteine prodotte dalle cellule per difendersi dall’invasione di un virus. Si chiamano così perché si formano per l’interferenza reciproca tra il virus e la cellula. (Fonte Focus)
Oltre alla capacità di conferire resistenza a molti virus, hanno quella di inibire la crescita di cellule normali e maligne (tumorali) e di modulare le funzioni di diverse cellule del sistema di difesa dell’organismo (sistema immunitario).
Fanno parte di una grande famiglia di proteine chiamate citochine, nome composto dalla radice cito-cellula e chinetico/cinetico (dal greco κινέω «muovere, mettere in movimento»).
Sono, quindi, molecole che diffondendosi nei tessuti e negli organi in cui vengono prodotte, o in cui sono trasportate dal circolo sanguigno, permettono la comunicazione a distanza tra le cellule attivando le più importanti linee di difesa immunitaria.
Per quanto riguarda il SARS-CoV-2…
Sembrerebbe che induca un immenso rilascio di interferone per cui, il tentativo dell’organismo di eliminare il virus nella maniera più “violenta” possibile, si trasforma in un’arma a doppio taglio per le persone con affezioni organiche e, probabilmente, anche per i giovani che (forse) non sanno di avere allergie respiratorie o con un sistema immunitario un po’ troppo “scalpitante”. In questi soggetti, la reazione immunitaria crea enormi disagi che, i nuovi farmaci sperimentali, stanno dimostrando di attenuare.
Le cellule che pare prediligere il SARS-CoV-2, nell’infezione, sono quelle polmonari, epatiche e dell’intestino tenue.
Da uno studio pubblicato su “ChinaXiv” dal Biologo Li Hua, le “spicole” (gli spuntoni della proteina “S”) siano molto attratte da un recettore attivato da un enzima dell’organismo ospite: la Furina.
Questa ipotesi, tuttavia, non convince l’intera comunità scientifica
Gli stessi gruppi di lavoro che studiano la Furina, stanno anche cercando molecole, in grado di disattivarla, che potrebbero servire come possibili terapie.
Altri ricercatori (come, ad esempio, Jason McLellan, biologo dell’Università del Texas ad Austin) invece, studiando approfonditamente la membrana delle cellule infettate stanno evidenziando ha dimostrato che la spicola del nuovo coronavirus si lega al recettore dell’angiotensina 2 (ACE2, che partecipa alla regolazione della pressione arteriosa) 10 volte più saldamente di come farebbe il virus della SARS.
Anche in questo caso, si stanno cercando farmaci in grado di “mascherare” questo recettore al Coronavirus.
Caratteristiche cliniche delle infezioni da Coronavirus umano (fonte NCBI – National Center for Biotechnology Information
Le caratteristiche cliniche delle infezioni CoV a bassa patogenicità non SARS sono indistinguibili da quelle riscontrate nei pazienti con virus influenzale (fino a 61.000 infezioni letali all’anno solo negli Stati Uniti secondo i Centers for Disease Control and Prevention). Come per le infezioni da influenza e virus respiratorio sinciziale (RSV), la maggior parte delle infezioni da CoV di solito porta a una sindrome simil-influenzale asintomatica o lieve. Quindi, senza diagnosi molecolare, queste malattie respiratorie virali, che seguono tutte un modello stagionale con una maggiore incidenza in inverno, sono classificate insieme come “influenza”, indipendentemente dalla loro esatta causa infettiva. Al contrario, il SARS-CoV altamente patogeno e il MERS-CoV hanno creato infezioni nefaste. I virus simili alla SARS sono scarsamente adattati all’ospite umano e, diversamente dai virus non SARS-CoV, sono generalmente associati a presentazioni cliniche più gravi.
ll SARS coronavirus-2 (SARS-CoV-2) appare altamente trasmissibile fra umani e capace di generare un ampio spettro di problematiche in pazienti con COVID-19 (la manifestazione clinica dell’infezione)
Diversi studi suggeriscono la possibilità che un gran numero di individui possano essere stati infettati da Coronavirus e hanno potenzialmente sviluppato un certo grado di risposta immunitaria (protettiva). Purtroppo non ci sono prove chiare sulla possibilità di una immunità permanente e adeguata contro altre specie di Coronavirus.” (fonte NCBI – National Center for Biotechnology Information)
I danni che il SARS-CoV-2 crea, sono legati, per lo più (come accennato prima) alla imponente risposta immunitaria che riguarda, come altre infezioni da Coronavirus tristemente famose (SARS e MERS) principalmente il sistema respiratorio e, anche quello enterico ed epatico
“La differenza principale fra i virus che causano un comune raffreddore e quelli che sono responsabili di infezioni più gravi consiste nel fatto che i primi colonizzano le vie aeree superiori, naso e gola, i secondi possono raggiungere i polmoni e causare polmonite” (I quaderni de Le Scienze marzo 2020)

“Nei casi più gravi causa una polmonite a focolai multipli localizzati nell’interstizio polmonare.( Lo spazio interstiziale è composto dalle pareti delle cavità aeree dei polmoni – gli alveoli e dagli spazi adiacenti ai vasi sanguigni e le piccole vie aeree. Le malattie polmonari interstiziali danno luogo a un anomalo accumulo di cellule infiammatorie nel tessuto polmonare, respiro affannoso e tosse)
A questo livello si realizza una reazione infiammatoria caratterizzata da infiltrato di linfociti, plasmacellule, macrofagi, leucociti e altre cellule che partecipano alla infiammazione. Tutto ciò provoca un ispessimento degli spazi interstiziali del polmone, il che impedisce il regolare svolgimento degli scambi gassosi ( ossigeno e anidride carbonica) tra capillare sanguigno che si trova nello spazio interstiziale e lo spazio alveolare del parenchima polmonare.
L’infezione virale in genere induce un’attivazione dei linfociti e delle plasmacellule che riconoscono il virus come agente estraneo al nostro organismo, per cui mettono in atto una reazione di difesa finalizzata all’eliminazione del “nemico”. Tutta questa reazione di difesa provoca l’infiammazione nell’interstizio polmonare da un lato, la produzione di anticorpi dall’altro. La reazione infiammatoria nell’interstizio polmonare si associa a produzione di sostanze chiamate citochine. Queste si distinguono in pro-infiammatorie e anti-infiammatorie. In questo caso prevalgono quelle pro-infiammatorie che causano la gravità del quadro patologico polmonare”. (dott. Pierluigi Frugiuele)
Ovviamente, non tutte le infezioni (da Coronavirus ma non solo) evolvono con manifestazioni cliniche e, soprattutto, si stanno utilizzando, in via sperimentale, ottimi farmaci che impediscono questa risposta immunitaria così intensa consentendo quindi una prognosi, in caso di malattia infettiva conclamata, decisamente più favorevole.
A questo punto, prima di concludere, è opportuno mostrare due immagini.
La prima (tratta dal libro “Argomenti di patologia generale” – Terranova / Giordano) riporta, a fumetti, il terreno di scontro fra degli agenti infettivi (in rosso) e tutto l’esercito del sistema immunitario (in blu)

La seconda, più scientifica, evidenzia il quadro funzionale del rapporto fra sistema nervoso, sistema endocrino (gli ormoni) e il sistema immunitario che la Psiconeuroendocrinoimmunologia spiega da molti anni.
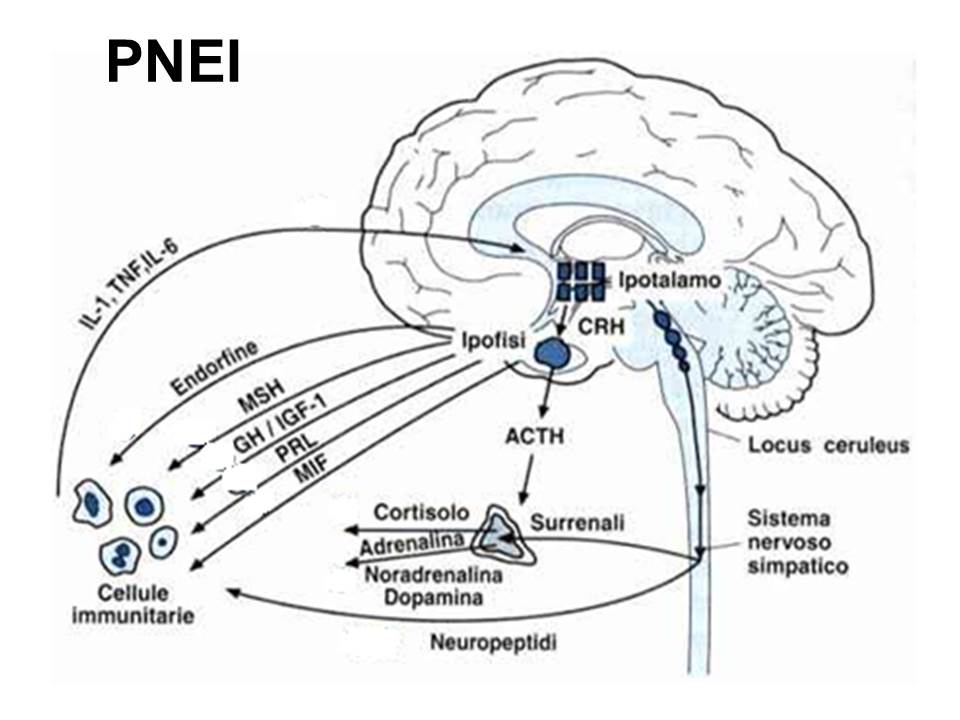
In pratica, questa branca scientifica, ci evidenzia un dato fondamentale: la miglior polizza assicurativa sulla vita che noi possiamo stipulare, è quella che ci porta ad avere una corretto rapporto ed equilibrio con noi stessi (nei limiti del possibile) che potrebbe essere alla base (al netto dei vari inquinanti atmosferici, di malattie pregresse “di comorbilità” e allergie più o meno evidenti) della differenza fra infezione e manifestazione clinica.
In conclusione, gli studi che contribuiscono a conoscere questo nuovo tipo di virus procedono ma non sono, al momento, completi. Ci spiegano che ci troviamo di fronte ad una gente infettivo “parente” di altri che, nel tempo abbiamo “addomesticato”. Giusto il tempo di arrivare alle stesse conclusioni.
Nel frattempo, sarà indispensabile rispettare i suggerimenti delle migliori fonti di informazione e divulgazione scientifica che, un po’ alla volta, cercheremo di sottoporre alla vostra attenzione, in questa rubrica.
BUONA RESILIENZA, CON UNA MIGLIORE CONOSCENZA
Ringrazio, molto, i colleghi medici, esperti in patologie respiratorie, Pierluigi Frugiuele (per la spiegazione offerta a proposito della patogenesi nella polmonite interstiziale) e Giacomo Bruni (per i suggerimenti bibliografici) e la dottoressa Ferdinanda Annesi, Biologa del CNR, per la consulenza e i suggerimenti bibliografici)
BIBLIOGRAFIA
- ^ Geller C, Varbanov M, Duval RE, Coronavirus umani: approfondimenti sulla resistenza ambientale e la loro influenza sullo sviluppo di nuove strategie antisettiche, in Viruses.
- ^ (EN) Liu P, Shi L, Zhang W, He J, Liu C, Zhao C, Kong SK, Loo JF, Gu D, Hu L, Prevalence and genetic diversity analysis of human coronaviruses among cross-border children, in Virology Journal, vol. 14, nº 1, November 2017, pp. 230, DOI:10.1186/s12985-017-0896-0, PMC 5700739, PMID 29166910.
- ^ Salta a:a b (EN) Forgie S, Marrie TJ, Healthcare-associated atypical pneumonia, in Seminars in Respiratory and Critical Care Medicine, vol. 30, nº 1, February 2009, pp. 67–85, DOI:10.1055/s-0028-1119811, PMID 19199189.
- FOCUS ON LINE – 12.03.2020
- PubMed – Coronavirus
- Bagga S, Bouchard MJ. Cell cycle regulation during viral infection. Methods Mol Biol. 2014;1170:165-227
- de Wilde AH et al. Host Factors in Coronavirus Replication. Curr Top Microbiol Immunol. 2018;419:1-42
- Enciclopedia Treccani
- Domande e risposte sui coronavirus a cura dell’Organizzazione Mondiale della Sanità
- Faq COVID-19 Ministero della Salute
- NCBI – National Center for Biotechnology Information
- Argomenti di patologia generale . T. terranova – D. Giordano (Società Editrice Universo – Roma)

Direttore Responsabile “La Strad@” – Medico Psicoterapeuta – Vicedirettore e Docente di Psicologia Fisiologica, PNEI & Epigenetica c/o la Scuola di Formazione in Psicoterapia ad Indirizzo Dinamico SFPID (Roma/ Bologna / Bari) – Presidente NEVERLANDSCARL e NEVERLAND “CAPELLI D’ARGENTO” ETS (a favore di un invecchiamento attivo e a sostegno dei caregiver per la Resilienza nel Dolore Sociale) – Responsabile Progetto SOS Alzheimer realizzato da NEVERLAND “CAPELLI D’ARGENTO” ONLUS – Responsabile area psicosociale dell’Ambulatorio Popolare (a sostegno dei meno abbienti) nel Centro Storico di Cosenza – Componente “Rete Centro Storico” Cosenza – Giornalista Pubblicista – CTU Tribunale di Cosenza.
Pagina personale
Canale youtube:

